アルミ電解コンデンサー(8)―― 市場不良と四級塩問題:中堅技術者に贈る電子部品“徹底”活用講座(41)(3/4 ページ)
四級塩問題のメカニズム
ではなぜ『通電の有無にかかわらず負極端子部のみに液漏れが発生』するのでしょうか?
決定的な詳しい原因は今でも公開されていませんが考えられる違いとしては陽極箔には化成(酸化膜)処理がされており、陰極箔はエッチングされた純アルミ箔という点があります。
特に純アルミは異種金属と接触すると水分によって電解腐食が発生するほど活性が高い金属です。この反応はアルミ合金内の不純物によっても発生しますので不純物の濃度にも注意する必要があります。
この陰極アルミ箔に取り付けられているアルミ合金のリード端子には不純物としての微量(0.05wt%以下)の鉄成分が含まれていますが、鉄とアルミとは溶けあわない(合金を作らない)ので鉄成分は鉄-アルミの金属間化合物(FeAlX)の形で局所的に存在することになります。
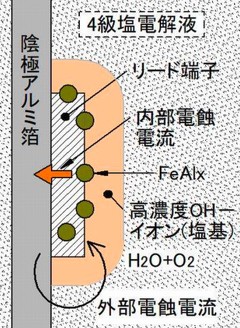
この状態で電解液に接触すると図2に示すようにアルミ箔からFeAlX方向へ電解液を介して電蝕電流が流れます。
接合部では次のようにアルミからFeAlXへ電子が供給されますので金属内部では
FeAlX→アルミ方向へ、そして電解液中ではアルミ箔→FeAlX方向へ電蝕電流が流れ、アルミ箔側で陽極反応、FeAlX側で陰極反応が起こることになります。
この反応により次のようにアルミ箔側には陽極酸化と同様に酸化膜が生成されますがこの酸化膜は不働態ですのでやがて反応電流(電蝕電流)は減少します。
しかし意図した良質な酸化膜ではありませんので一部の電蝕電流は永続的に流れ、この反応は弱くなりながらも持続されます。
一方、リード端子のFeAlX側では電解液中の水分と酸素で1式に表す陰極反応が起こります。なお酸素O2は封口ゴムの分子間を通じて大気中から供給されます。
アニオン(酸)=H++陰イオン
カチオン(塩基)=陽イオン+OH−
塩=アニオン+カチオンの化合物
この結果、FeAlX近傍には6個の水酸化物イオン(OH−)が存在し、水素イオン濃度を上回りますので塩基性を示し、一部は陽イオンと結合して塩基になります(図2)。
同様の現象は小学校などで行う理科の海水(=塩水、NaCl+H2O)の電気分解実験において陰極近傍が塩基性になることがフェノールフタレイン溶液で確認できます。
この水酸化物イオンや塩基は再び電解液中に拡散し、中和されていきますがリード端子近傍の拡散しきれない分が封口ゴムに接触するとゴムは膨潤、劣化して密着性を失い、この塩基性溶液や塩基が漏れることになります。
特に低圧箔は面積拡大のための交流エッチングで不純物がふるい落とされてアルミ純度が高まっているのでこのような現象が強く起きる可能性が高くなります。
上記のような反応が四級塩を使った電解コンデンサーの中で起きていると考えられます。この考え方(推論)は次の事象とも合致します。
- 強固な酸化膜を持つ正極端子側では発生していない。
- 酸素を窒素で置き換えた雰囲気中での実験ではこのような液漏れ現象が発生しない。⇒1式の酸素が大きな因子を占めている。
- 漏れた液体の成分がFeAlXを含む塩基である。
(注)従来の環状アミジン塩では陰極近傍の水酸化物イオン(OH−)を取り込んでOH−イオン濃度を減少させ、自身は弱い塩基成分に変化するという反応によって陰極付近の塩基性を抑制しますが事故を起こした第四級塩にはこのような作用がないようです。
対策
このような流れから対策としては、
- 正極、負極とも酸化膜を使用する。
- 電解液中の水分を“0”にする。
- 生成される塩基と封口ゴムとの相性を再検討する。
- リード端子に含まれる不純物を極限まで取り除いた材料を使用する。
- リード端子にアルミと電蝕を起こさない表面処理を施す。
などが考えられます。実際に一部の電気2重層キャパシターなどでは四級塩(テトラエチルアンモニウムTEA※も汎用的に使われています。(Wikipedia 2019年6月13日(木)15:27版)
※テトラエチルアンモニウム(TEA英文WikiPedia Tetraethylammonium 3 February 2020, at 23:28)
内部窒素窒素原子に結合した4つのエチル基からなる第四級アンモニウムカチオンであり、正に帯電しています。
・参考資料:アルミ電解コンデンサにおけるマイナス端子側塩基性成分の集中メカニズム[PDFデータ]
Copyright © ITmedia, Inc. All Rights Reserved.
記事ランキング
- マイコンの通信機能 UARTとI2C 、SPIの違い
- 校正やテストに使える 2線式ループ電流発生器を作ってみた
- 「分解能0.1%」の静電容量式位置センサーを構成する
- ダイヤモンド半導体用2インチウエハー量産へ モザイク結晶開発に成功
- 熱間加工磁石で材料ロス低減 EVモーター用ローター
- ON/OFFコンバーターの制御不安定問題(3)状態平均化法での結果と安定化動作に必要な位相/利得
- 次世代データセンター向け1200V SiC MOSFET、オン抵抗58%削減
- NAND/NORフラッシュメモリの違いと記録方式を分かりやすく解説
- 車両のコア機能を「一元管理」 NXPの新車載プロセッサ
- ARM台頭にルネサス誕生……時代に翻弄され続けた日立「SuperH」